- · 《生命科学仪器》编辑部[10/30]
- · 《生命科学仪器》杂志社[10/30]
- · 《生命科学仪器》期刊栏[10/30]
- · 《生命科学仪器》数据库[10/30]
- · 《生命科学仪器》投稿方[10/30]
- · 生命科学仪器版面费是多[10/30]
1天深圳大学/山西大学等单位连发5篇Nature,在生(3)
作者:网站采编关键词:
摘要:图2:GABAB受体采取非对称性变化的激活机制 GABAB主要通过3个胞内环偶联Gi蛋白:其中较长的ICL2主要与G蛋白上α5,αN,β2-β3的结合,占据了约80%的互作界面
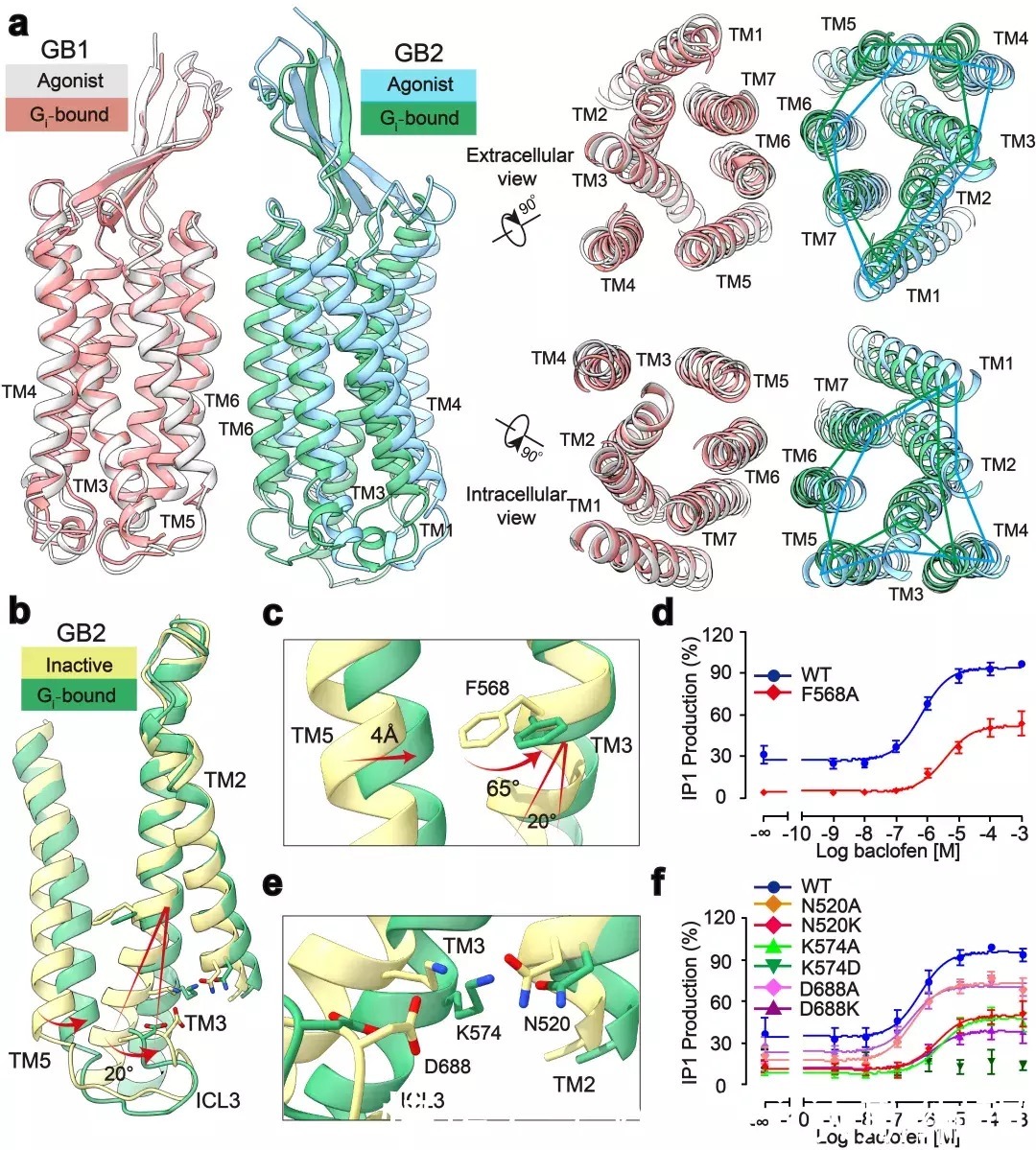
图2:GABAB受体采取非对称性变化的激活机制
GABAB主要通过3个胞内环偶联Gi蛋白:其中较长的ICL2主要与G蛋白上α5,αN,β2-β3的结合,占据了约80%的互作界面;而较短的ICL1、ICL3主要与G蛋白的α5末端几个氨基酸相互作用,稳定了G蛋白的结合(图3a,b)。此外研究发现GABAB受体选择性识别Gi/o亚型G蛋白是由于Gi/o的H5.23位点是小侧链的半胱氨酸,而Gs、Gq等类型G蛋白的相应位置大侧链的酪氨酸与GABAB受体具有潜在的空间位阻(图3c)。
功能实验分析发现,当把H5.23位点的半胱氨酸突变成大侧链的色氨酸后,其偶联G蛋白的能力显著降低,而当突变成小侧链的丙氨酸后,其结合G蛋白的能力没有变化(图3d,e)。
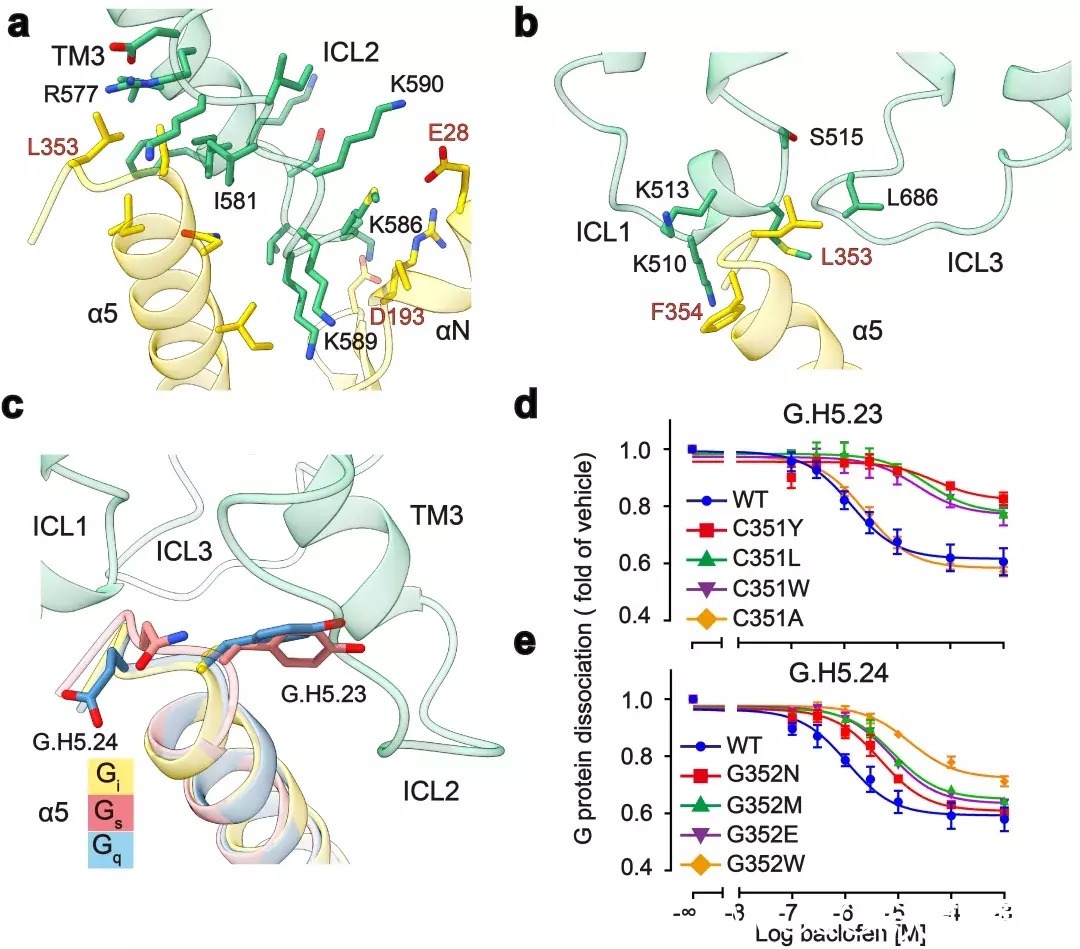
图3:GABAB受体选择性偶联Gi蛋白的分子机制
该项工作完整地阐述了C型异源二聚体GABAB受体的非对称激活机制:在非激活状态下,GABAB受体两个亚基的VFT区都处于开放状态,TM区采用TM3-TM5/TM3-TM5互作界面;激动剂结合GB1-VFT正位口袋后,诱导GB1-VFT闭合,从而使得GB2-VFT旋转,进一步由颈区传导至TM结构域的重排,形成新的TM6/TM6作用界面;PAM以及G蛋白的结合,进一步诱导了GB2的TM区的旋转,形成更稳定的TM6/TM6互作界面;此外GB2亚基F568等残基精细的构象变化,导致其TM3/TM5的胞内端外移,三个胞内环形成较浅的口袋选择性偶联Gi/o蛋白,最终激活下游信号通路(图4)。
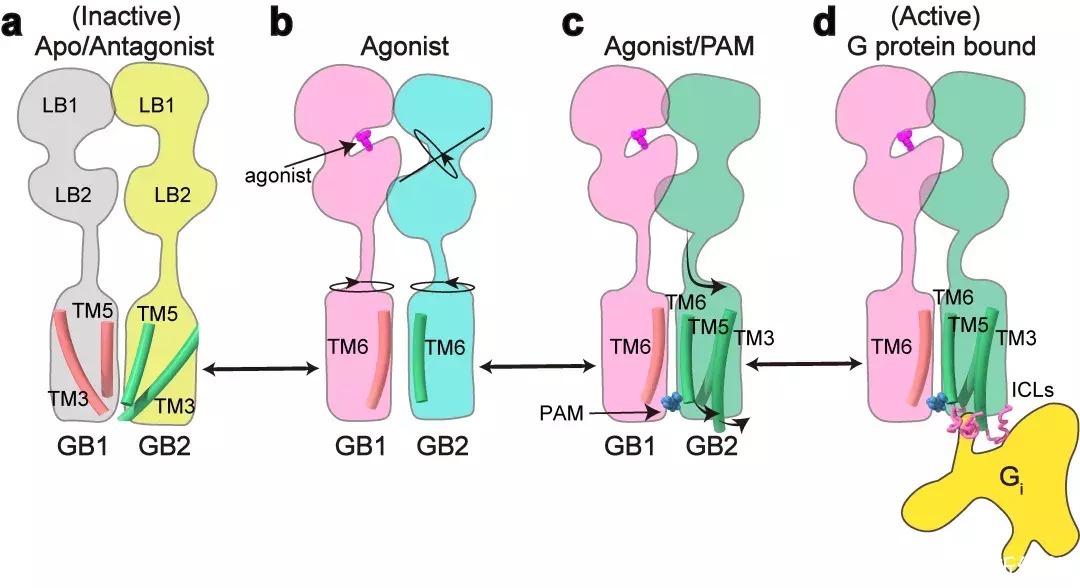
图4:GABAB受体激活的信号转导模型
本研究是浙江大学—华中科技大学细胞信号转导联合实验室在C型GPCR信号转导机制研究中的又一重大突破。该工作也进一步验证了刘剑峰课题组之前发现的C型GPCR二聚体,如代谢型谷氨酸受体(Nat Chem Biol.,2015;?PNAS., 2011),GABAB受体(Cell Research,2020;?Nat Commun.,2019;EMBO J.,2008)和钙敏感受体(PNAS.,2020)中不同亚基的各个功能域变构调节的激活模式。
华中科技大学与浙江大学医学院联合培养博士生申仓松、浙江大学医学院附属邵逸夫医院毛春友研究员、华中科技大学教师许婵娟和博士生晋楠为本研究第一作者。华中科技大学生命科学与技术学院刘剑峰教授,浙江大学医学院张岩研究员和法国功能基因研究所PIN JP教授为共同通讯作者。
浙江大学医学院蛋白质平台、冷冻电镜中心为本次研究的样品制备和数据收集提供了支持。该工作也得到了浙江中医药大学陈忠教授,浙江大学药学院侯廷军教授和法国功能基因研究所Rondard P教授的协助。本工作得到了科技部国家重点研发计划、国家自然科学基金等项目的大力支持。
版权声明:本文转自“iNature”,文章转载只为学术传播,不代表本号观点,无商业用途,版权归原作者所有,如涉及侵权问题,请联系我们,我们将及时修改或删除。
WOSCI沃斯编辑,耶鲁大学博士团队匠心打造,专注最新科学动态并提供各类科研学术指导,包括:前沿科学新闻、出版信息、期刊解析、SCI论文写作技巧、学术讲座、SCI论文润色等。
文章来源:《生命科学仪器》 网址: http://www.smkxyq.cn/zonghexinwen/2021/0513/550.html
上一篇:汇友生命科学(08088)已向上市复核委员会提供书面
下一篇:汇友生命科学(08088)预期一季度亏损收窄40%至50%